Διαφορές γενετικών και επιγενετικών δεικτών
Οι γενετικοί και οι επιγενετικοί δείκτες των τεστ μεθυλίωσης αποτελούν κρίσιμα εργαλεία για την κατανόηση των βιολογικών διεργασιών, ωστόσο λειτουργούν με θεμελιωδώς διαφορετικούς τρόπους. Οι γενετικοί δείκτες είναι παραλλαγές στις αλληλουχίες του DNA που μπορούν να κληρονομηθούν άμεσα και είναι συνήθως σταθερές καθόλη τη διάρκεια της ζωής ενός οργανισμού. Αυτές οι παραλλαγές περιλαμβάνουν πολυμορφισμούς ενός νουκλεοτιδίου (SNPs), προσθήκες, διαγραφές και παραλλαγές στον αριθμό αντιγράφων [11, 12].
Η ταυτοποίηση των γενετικών δεικτών επιτρέπει τον προσδιορισμό του τύπου του HPV και τη σύνδεσή του με πιθανές οδούς ανάπτυξης της νόσου, όπως η ανάπτυξη καρκίνου του τραχήλου της μήτρας [13, 14]. Για παράδειγμα, η παρουσία τύπων HPV υψηλού κινδύνου, ιδίως HPV16 και HPV18, αξιολογείται με τη χρήση μεθόδων PCR ή άλλων μοριακών τεχνικών που ανιχνεύουν συγκεκριμένες γονιδιωματικές αλληλουχίες [15]. Αυτοί οι γενετικοί δείκτες είναι σε μεγάλο βαθμό σταθεροί και παρέχουν μια σαφή γενετική υπογραφή που σχετίζεται με τη λοίμωξη από HPV και τον κίνδυνο ανάπτυξης όγκων.
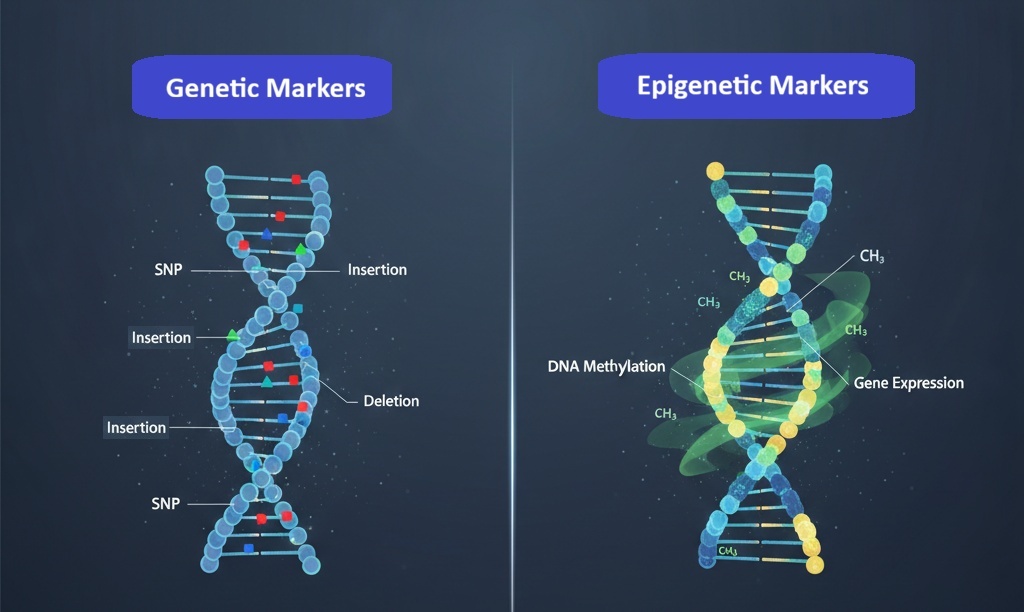
Αντίθετα, οι επιγενετικοί δείκτες, ιδιαίτερα η μεθυλίωση του DNA, αναφέρονται σε τροποποιήσεις που δεν αλλοιώνουν την υποκείμενη αλληλουχία του DNA, αλλά μπορούν να επηρεάσουν σημαντικά την έκφραση των γονιδίων και τη κυτταρική λειτουργία [16, 17]. Αυτοί οι δείκτες μπορούν να επηρεαστούν από περιβαλλοντικούς παράγοντες, στάδια ανάπτυξης και τον τρόπο ζωής (διατροφή, κάπνισμα, άσκηση κ.ά), οδηγώντας σε αναστρέψιμες αλλαγές που μπορούν να κληρονομηθούν από γενιά σε γενιά [18, 19, 20]. Για παράδειγμα, διαφορετικά μοτίβα μεθυλίωσης του DNA μπορούν να εμφανιστούν στα σωματικά κύτταρα γενετικά πανομοιότυπων οργανισμών, αποδεικνύοντας πώς εξωτερικά ερεθίσματα μπορούν να προκαλέσουν σημαντικές αλλαγές στη ρύθμιση των γονιδίων χωρίς να αλλοιώσουν τον ίδιο το γενετικό κώδικα [21, 22,23].

Στην περίπτωση του HPV, τα μη φυσιολογικά μοτίβα μεθυλίωσης έχουν συσχετιστεί με την εξέλιξη της λοίμωξης από HPV σε παθολογικές καταστάσεις όπως η ενδοεπιθηλιακή νεοπλασία του τραχήλου της μήτρας (CIN) και ο καρκίνος του τραχήλου της μήτρας [13, 24]. Η μεθυλίωση συγκεκριμένων γονιδίων του HPV, όπως το γονίδιο L2, έχει δείξει δυνατότητες ως βιοδείκτης για την αναγνώριση βλαβών υψηλού βαθμού. Τα μη φυσιολογικά μοτίβα μεθυλίωσης μπορούν να υποδηλώνουν τη επιθετικότητα της λοίμωξης από HPV και την ικανότητά της για εξέλιξη σε κακοήθεια [25]. Επιπλέον, αυτοί οι επιγενετικοί δείκτες μπορούν να επηρεαστούν από περιβαλλοντικούς παράγοντες, γεγονός που τους καθιστά ελκυστικούς στο πλαίσιο της εξατομικευμένης ιατρικής για τον έλεγχο και την παρακολούθηση του καρκίνου του τραχήλου της μήτρας [26, 27].
Η σημασία των επιγενετικών δεικτών στη διάγνωση HPV-σχετιζόμενων αλλοιώσεων
Οι επιγενετικοί δείκτες, ιδιαίτερα τα μοτίβα μεθυλίωσης του DNA, διαδραματίζουν ουσιαστικό ρόλο στη διάγνωση και την πρόγνωση των ασθενειών που σχετίζονται με τον HPV, ιδίως του καρκίνου του τραχήλου της μήτρας. Για παράδειγμα, μια μελέτη έδειξε ότι συγκεκριμένα μοτίβα μεθυλίωσης του DNA μπορούσαν να προβλέψουν την κλινική πρόγνωση των ασθενών με καρκίνο του τραχήλου της μήτρας, υπογραμμίζοντας το δυναμικό τους ως βιοδείκτες για την παρακολούθηση της νόσου [28].

Έρευνες έχουν δείξει ότι τα υψηλότερα επίπεδα μεθυλίωσης συσχετίζονται με την ανάπτυξη υψηλού βαθμού ενδοεπιθηλιακής νεοπλασίας του τραχήλου της μήτρας (CIN) και διηθητικού καρκίνου του τραχήλου της μήτρας, παρέχοντας ένα μηχανισμό μέσω του οποίου η μεθυλίωση μπορεί να χρησιμεύσει ως κρίσιμο διαγνωστικό εργαλείο [13]. Η ικανότητα ανίχνευσης τέτοιων αλλαγών μεθυλίωσης ενισχύει την ευαισθησία και την ειδικότητα των μεθοδολογιών εξέτασης HPV και μπορεί να βοηθήσει στη διάκριση μεταξύ παροδικών λοιμώξεων και εκείνων που είναι πιο πιθανό να οδηγήσουν σε κακοήθεια [29].
[11] Chim, S. S., Tong, Y. K., Chiu, R. W., Lau, T. K., Leung, T. N., Chan, L. Y., … & Lo, Y. D. (2005). Detection of the placental epigenetic signature of the maspin gene in maternal plasma. Proceedings of the National Academy of Sciences, 102(41), 14753-14758.
[12] Heyn, H., Moran, S., Hernando-Herraez, I., Sayols, S., Gomez, A., Sandoval, J., … & Esteller, M. (2013). DNA methylation contributes to natural human variation. Genome research, 23(9), 1363-1372.
[13] Mirabello, L., Schiffman, M., Ghosh, A., Rodriguez, A. C., Vasiljevic, N., Wentzensen, N., … & Lorincz, A. T. (2013). Elevated methylation of HPV16 DNA is associated with the development of high grade cervical intraepithelial neoplasia. International journal of cancer, 132(6), 1412-1422.
[14] Gilham, C., Nedjai, B., Scibior‐Bentkowska, D., Reuter, C., Banwait, R., Brentnall, A. R., … & Lorincz, A. T. (2024). Long‐term prediction by DNA methylation of high‐grade cervical intraepithelial neoplasia: Results of the ARTISTIC cohort. International journal of cancer, 155(1), 81-92.
[15] Radhakrishna, U., Albayrak, S., Zafra, R., Baraa, A., Vishweswaraiah, S., Veerappa, A. M., … & Bahado-Singh, R. O. (2019). Placental epigenetics for evaluation of fetal congenital heart defects: Ventricular Septal Defect (VSD). PloS one, 14(3), e0200229.
[16] Mohtat, D., & Susztak, K. (2010, September). Fine tuning gene expression: the epigenome. In Seminars in nephrology (Vol. 30, No. 5, pp. 468-476). WB Saunders.
[17] Salozhin, S. V., Prokhorchuk, E. B., & Georgiev, G. P. (2005). Methylation of DNA—one of the major epigenetic markers. Biochemistry (Moscow), 70(5), 525-532.
[18] Han, Z., Crisp, P. A., Stelpflug, S., Kaeppler, S. M., Li, Q., & Springer, N. M. (2018). Heritable epigenomic changes to the maize methylome resulting from tissue culture. Genetics, 209(4), 983-995.
[19] Eichten, S. R., Swanson-Wagner, R. A., Schnable, J. C., Waters, A. J., Hermanson, P. J., Liu, S., … & Springer, N. M. (2011). Heritable epigenetic variation among maize inbreds. PLoS Genetics, 7(11), e1002372.
[20] Law, P. P., & Holland, M. L. (2019). DNA methylation at the crossroads of gene and environment interactions. Essays in biochemistry, 63(6), 717-726.
[21] Stelpflug, S. C., Eichten, S. R., Hermanson, P. J., Springer, N. M., & Kaeppler, S. M. (2014). Consistent and heritable alterations of DNA methylation are induced by tissue culture in maize. Genetics, 198(1), 209-218.
[22] Feng, S., Cokus, S. J., Zhang, X., Chen, P. Y., Bostick, M., Goll, M. G., … & Jacobsen, S. E. (2010). Conservation and divergence of methylation patterning in plants and animals. Proceedings of the National Academy of Sciences, 107(19), 8689-8694.
[23] Martos, S. N., Tang, W. Y., & Wang, Z. (2015). Elusive inheritance: transgenerational effects and epigenetic inheritance in human environmental disease. Progress in biophysics and molecular biology, 118(1-2), 44-54.
[24] Sun, C., Reimers, L. L., & Burk, R. D. (2011). Methylation of HPV16 genome CpG sites is associated with cervix precancer and cancer. Gynecologic oncology, 121(1), 59-63.
[25] Sonar, S., Nyahatkar, S., Kalele, K., & Adhikari, M. D. (2024). Role of DNA methylation in cancer development and its clinical applications. Clinical and Translational Discovery, 4(1), e279.
[26] Pun, P. B., Liao, Y. P., Su, P. H., Wang, H. C., Chen, Y. C., Hsu, Y. W., … & Lai, H. C. (2015). Triage of high-risk human papillomavirus-positive women by methylated POU4F3. Clinical epigenetics, 7(1), 85.
[27] Ladoukakis, E., Andriamiadana, G., Hajizadah, F., James, L. G., & Nedjai, B. (2025). Epigenetic Biomarkers for Cervical Cancer Progression: A Scoping Review. International Journal of Molecular Sciences, 26(19), 9423.
[28] Zhou, R., Chen, Z., Xiao, Z. R., Wang, S. L., & Rong, C. (2021). HPV-related promoter methylation-based gene signature predicts clinical prognosis of patients with cervical cancer. Frontiers in Oncology, 11, 753102.
[29] Brentnall, A. R., Vasiljević, N., Scibior‐Bentkowska, D., Cadman, L., Austin, J., Szarewski, A., … & Lorincz, A. T. (2014). A DNA methylation classifier of cervical precancer based on human papillomavirus and human genes. International journal of cancer, 135(6), 1425-1432.
